9.E4 : Taux d’avancement avec une réaction d’oxydoréduction
Données : \(\ce{Ag+(aq) / Ag(s)}\) ; \(\ce{Cu^2+(aq) / Cu(s)}\) ; \(M(\ce{Cu}) = \pu{63,5 g*mol–1}\).
Un fil de cuivre \(\ce{Cu(s)}\) de masse \(m_{Cu}= \pu{5,0 g}\) est plongé dans une solution de volume \(V = \pu{100 mL}\) contenant des ions argent \(\ce{Ag+(aq)}\) telle que \([\ce{Ag+}] = \pu{0,075 mol*L–1}\). La solution se colore en bleu et un dépôt d’argent se forme sur le cuivre. L’absorbance, à \(λ = \pu{500 nm}\), de la solution obtenue est égale à \(\pu{0,47}\).
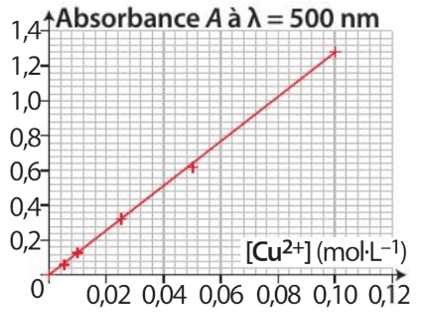
1 Écrire l’équation de la réaction.
2 À l’aide du taux d’avancement, conclure quant au caractère total ou non de la transformation.
