13.E5 : Isomères ou non...
L’éphédrine est utilisée dans divers pays pour le traitement de l’asthme, de l’obésité ou lors d’interventions chirurgicales pour maintenir une pression artérielle suffisamment haute. Proche chimiquement des amphétamines, elle est utilisée à des fins de dopage chez les sportifs de haut niveau. Son usage est donc régulé dans de nombreux pays.
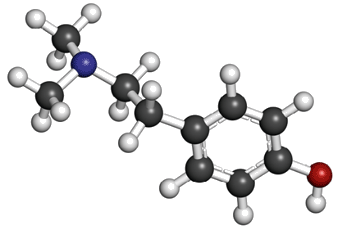
L’hordénine est une molécule analogue extraite de l’orge. En infusion, elle permet de traiter la diarrhée.
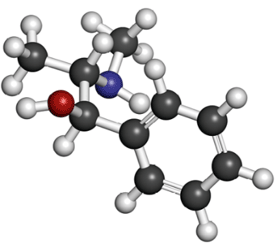
1 Déterminer la formule brute de l’éphédrine.
2 Représenter sa formule topologique. Entourer et nommer ses groupes caractéristiques.
3 Préciser combien l'éphédrine possède de doubles liaisons.
4 Déterminer la formule brute et représenter la formule topologique de l’hordénine. Conclure.
