2.E3 : L'éthanal
On donne ci-dessous, le schéma de Lewis de la molécule d'éthanal.
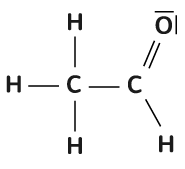
Justifier si l’éthanal peut être un acide.
Données :
• Électronégativités de quelques éléments : \(\chi(H) = \pu{2,2}\) ; \(\chi(C) = \pu{2,55}\) ; \(\chi(O) = \pu{3,44}\)
• Propriété : Une liaison est polarisée si les atomes mis en jeu ont une différence d'électronégativités supérieure à \(\pu{0,5}\).