1.E4 : Deux cafés s'il vous plaît !
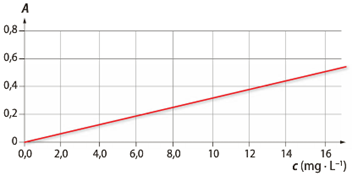
On souhaite doser la caféine dans deux tasses de café notées 1 et 2. Pour cela, on prépare des solutions de caféine de concentrations massiques \(\pu{4,0 mg*L–1}\), \(\pu{8,0 mg*L–1}\), \(\pu{12 mg*L–1}\) et \(\pu{16 mg*L–1}\). Le spectre d’absorption de la caféine est donné ci-dessous. On mesure par ailleurs l’absorbance des solutions étalons à \(\pu{271 nm}\) et on obtient la courbe d’étalonnage ci-dessous.
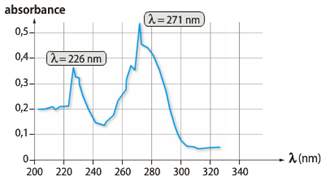
1 Pourquoi mesure-t-on l’absorbance des solutions étalons à \(\pu{271 nm}\) ?
2 Justifier l’allure de la courbe d’étalonnage.
3 À \(\pu{271 nm}\), les absorbances des deux cafés valent \(A_1=\pu{0,17}\) et \(A_2= \pu{0,53}\).
3.a Quel est le café qui contient le plus de caféine ?
3.b Quelles sont les concentrations en caféine des deux cafés ?
4 Déterminer la concentration de la solution qui a été utilisée pour réaliser le spectre d’absorbance.